2025年5月16日���,球速体育(2696.HK)宣布���,公司自主研制的伊匹木单抗生物类似药HLX13(重组抗CTLA-4全人单克隆抗体注射液)的I/III期临床研究(NCT06841185)在中国完成首例受试者给药。球速体育已于2025年4月与Sandoz达成授权许可合作���,授予Sandoz对HLX13在美国���、欧洲42个国家和地区���、日本���、加拿大及澳大利亚的独家商业化权益。
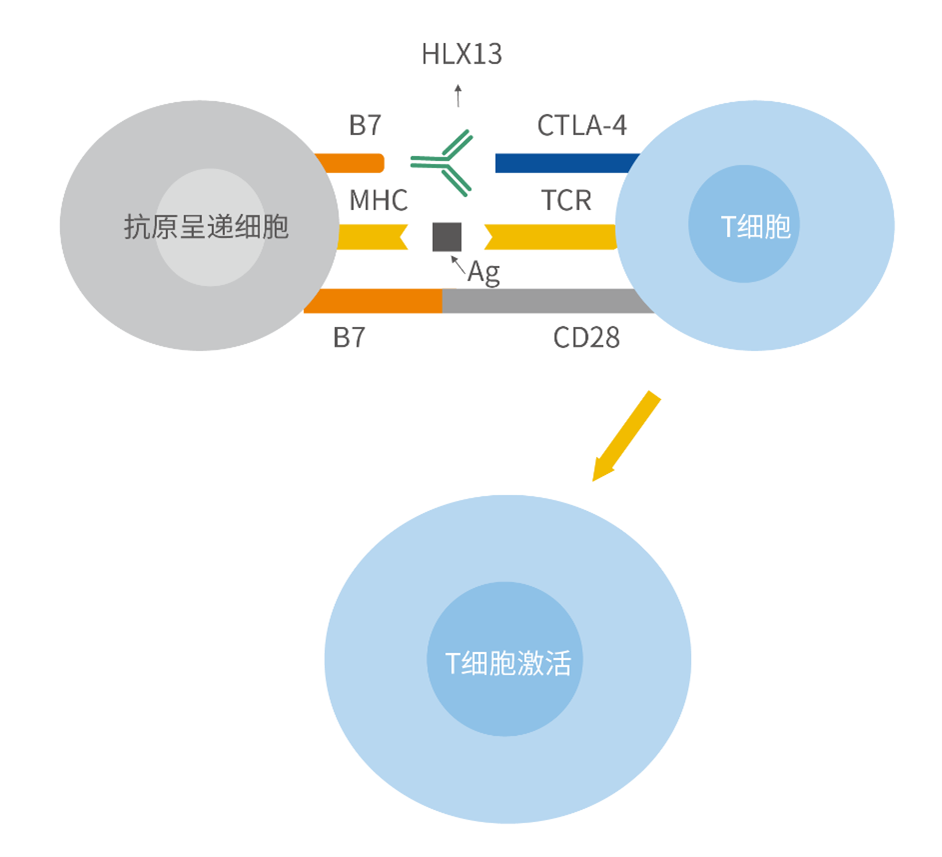
近年来���,免疫疗法为肿瘤治疗提供了新的途径���,具有独特的优势和巨大的潜力。肿瘤免疫检查点抑制剂是肿瘤免疫治疗中的重要组成部分[1]。与PD-1/L1���、LAG-3相似���,细胞毒性T淋巴细胞相关抗原4(cytotoxic T-lymphocyte-associated protein 4, CTLA-4)也是一类免疫抑制型检查点蛋白���,主要表达在调节性T细胞和活化的T细胞上。与CD28相比���,CTLA-4对B7分子的亲和力更强���,通过与CD28竞争性结合抗原呈递细胞上的B7配体(B7-1和B7-2)���,抑制T细胞的增殖和活化[2]。全人抗CTLA-4单克隆抗体能够解除CTLA-4对T细胞活化所需的共刺激信号的抑制���,增加活性效应T细胞的数量���,从而动员 T 细胞对肿瘤细胞发动直接免疫攻击。此外���,抗CTLA-4单抗可选择性地耗尽肿瘤部位的调节T细胞���,导致肿瘤内效应T细胞/调节T细胞的比例增加���,从而导致肿瘤细胞死亡。研究证明���,伊匹木单抗注射液与PD-1抑制剂组成的双免疫联合疗法能够产生协同的抗肿瘤效果���,为患者带来更大的临床获益[3-4]。截至目前���,伊匹木单抗联合纳武利尤单抗已在全球多个国家和地区获批���,适应症包括联合纳武利尤单抗用于黑色素瘤���、肝细胞癌等一系列适应症。
HLX13(抗CTLA-4单抗)药理作用示意图
HLX13是球速体育严格按照中国���、欧盟和美国等生物类似药法规自主研发的伊匹木单抗注射液生物类似药���,有望用于多种实体瘤的治疗。公司已经完成了HLX13与原研药伊匹木单抗注射液的药学���、临床前药理学���、毒理学和药代动力学全面对比研究���,上述临床前研究未发现HLX13与原研药伊匹木单抗注射液存在显著差异。
未来���,球速体育还将持续立足于未满足的临床需求���,充分发挥公司在抗体药物和抗体偶联药物领域的一体化平台优势���,持续探索免疫治疗在肿瘤中的治疗潜力���,为全球患者带来更多高质量���、可负担的创新治疗方案。
关于NCT06841185
本研究为一项多中心���、随机���、双盲���、平行对照1/3期临床研究���,旨在评估HLX13与其原研药YERVOY®(美国市售和欧盟市售)在既往未经治疗的不可切除的晚期肝细胞癌(HCC)患者中的药代动力学(PK)特征���、有效性���、安全性和免疫原性相似性。合格的受试者将按2:1:1的比例随机分配至三组���,在前4个周期���,受试者每3周接受一次HLX13���、美国市售的YERVOY®或欧盟市售的YERVOY®治疗���,三组均联合纳武利尤单抗。随后每4周接受一次纳武利尤单抗治疗���,最多10个周期。主要PK终点为从给药前至首次给药后21天的血药浓度-时间曲线下面积(AUC0-21d)和稳态给药间隔内血药浓度-时间曲线下面积(AUCss);主要有效性终点为由独立放射学审查委员会(IRRC)根据实体肿瘤临床疗效评价标准(RECIST v1.1)评估的直至第24周的最佳客观缓解率(ORR)。次要终点包括其他PK参数���、其他有效性评估���、安全性及免疫原性。
